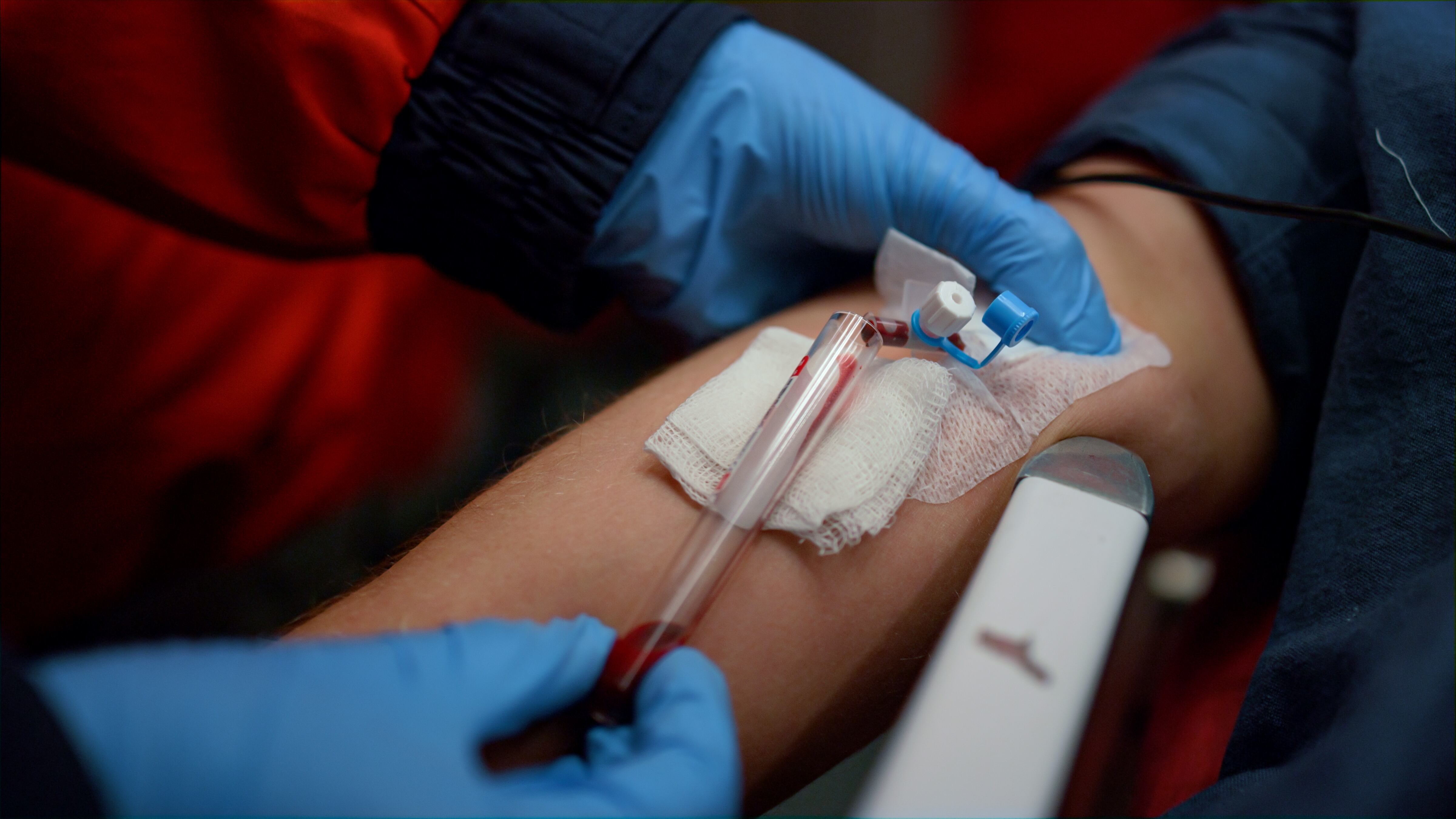
Un sensor óptico desarrollado en la Universidad de Shenzhen, utilizando CRISPR y puntos cuánticos, permite detectar biomarcadores de cáncer en sangre a niveles muy bajos sin necesidad de amplificación química, lo que podría mejorar el diagnóstico temprano. El dispositivo fue probado con un biomarcador asociado al cáncer de pulmón, según un estudio publicado en la revista Óptica.
Detectar un cáncer cuando todavía “no se ve” en una tomografía es uno de los grandes objetivos de la medicina de precisión. El problema es conocido: en etapas iniciales, los tumores liberan al torrente sanguíneo cantidades minúsculas de biomarcadores —proteínas, ADN/ARN circulante u otras moléculas— y la señal suele quedar enterrada en el ruido del propio suero. Por eso, muchos métodos actuales recurren a pasos de amplificación química (más tiempo, más coste y más complejidad).
Un equipo liderado por Han Zhang, de la Univ ”, es decir, tan bajas que en la práctica equivalen a detectar apenas unas pocas moléculas en la muestra. La investigación se publicó en la revista Óptica y fue difundida el 12 de febrero del 2026.
¿Cómo funciona el dispositivo?
La clave es una técnica fotónica llamada generación de segundo armónico (SHG, por sus siglas en inglés). En términos simples, el sistema ilumina una superficie y “convierte” parte de esa luz en otra de la mitad de longitud de onda; el cambio puede medirse con gran sensibilidad. En este trabajo, la SHG se produce en la superficie de un semiconductor bidimensional: el disulfuro de molibdeno (MoS₂).
Sobre ese material, los investigadores construyen una nanoarquitectura híbrida: tetraedros de ADN (pequeñas estructuras autoensambladas con forma piramidal) que colocan puntos cuánticos a distancias controladas del MoS₂. Los puntos cuánticos refuerzan el campo óptico local y, con ello, intensifican la señal SHG sin necesidad de los pasos clásicos de amplificación química.
La selectividad la aporta CRISPR-Cas12a. Cuando el sistema reconoce el biomarcador objetivo, Cas12a corta el ADN que mantiene sujetos los puntos cuánticos; ese corte se traduce en una caída medible de la señal SHG. Como la SHG tiene un fondo (ruido) muy bajo, la lectura final gana precisión en condiciones donde otros enfoques se vuelven ambiguos.
Ensayo con un biomarcador de cáncer de pulmón
Para demostrar la utilidad clínica, el equipo eligió miR-21, un microARN frecuentemente estudiado como biomarcador asociado a cáncer de pulmón. Primero validaron la detección en soluciones tampón y luego en suero humano de pacientes con cáncer de pulmón, simulando un escenario de análisis de sangre real. El sensor no solo detectó miR-21 a niveles ultrabajos, sino que además discriminó la diana frente a hebras de ARN similares, un punto crítico para evitar falsos positivos.
De la bancada al hospital: lo que falta
Los autores subrayan que el siguiente paso es miniaturizar el montaje óptico para convertirlo en un dispositivo portátil: usable “a pie de cama”, en clínicas o incluso en entornos con recursos limitados. Si esa ingeniería llega a buen puerto, la propuesta apunta a dos usos potentes: cribados tempranos (antes de que el tumor sea visible en una TC) y monitorización frecuente (diaria o semanal) de biomarcadores para evaluar respuesta a fármacos sin esperar meses a nuevas imágenes.
Además, al ser programable, el mismo enfoque podría adaptarse a otros objetivos biomoleculares: virus, bacterias, toxinas ambientales o biomarcadores vinculados a enfermedades neurodegenerativas. Aun así, como ocurre con toda “promesa” de detección temprana, el reto no será solo técnico: hará falta validación en cohortes más amplias, estandarización del muestreo y demostrar que detectar antes se traduce en mejores decisiones clínicas y resultados para el paciente.
En el ecosistema de las “biopsias líquidas”, la sensibilidad es el gran cuello de botella. Pruebas basadas en PCR o secuenciación pueden ser muy potentes, pero suelen exigir preparación de muestra y ciclos de amplificación para hacer visible lo invisible. El enfoque SHG propone “leer” directamente el evento molecular sobre una superficie, con menos pasos intermedios; a cambio, habrá que integrar la fotónica en un formato clínico robusto (estabilidad, calibración y repetibilidad) para que el resultado sea consistente fuera del laboratorio. Esa será la prueba decisiva antes de su adopción masiva.